Ursachen. Die Mechanismen, die zur Aorteninsuffizienz führen, können an der Klappe oder an der Aorta liegen.Die wichtigste angeborene Klappenabnormalität, die zu einer Aorteninsuffizienz führen kann, ist die bicuspide Klappe. Erworbene Klappenabnormalitäten sind Verkalkungen, Vegetationen, rheumatische Veränderungen und Schäden durch Strahlen und Toxine. Die wichtigsten angeborene Erkrankungen , die eine Aortendilatation und dadurch eine Aorteninsuffizienz verursachen können, sind das Marfan-Syndrom und das Ehlers-Danlos-Syndrom. Erworbene Aortenveränderungen entstehen idiopathisch, durch chronische arterielle Hypertonie, durch Autoimmunerkrankungen wie Lupus, durch Lues, durch Vaskulitiden wie die Takayasu-Aortis und traumatisch.
Bei einer bicuspiden Klappe kann eine Insuffizienz sowohl durch die vermehrte Belastung auf die vergrösstere Tasche als auch durch eine häufig mit biscupiden Klappen assoziierte Aortenektasie verursacht werden.
Die Einteilung nach Carpentier für die Mechanismen der Aorteninsuffizienz beschreibt Typ 1 ohne Bewegungsstörung der Taschen, Typ 2 durch erhöhte Bewegung (z.B. Prolaps) und Typ 3 durch verminderte Bewegung (z.B. bei degenerativen Verkalkung). Typ 1a, 1b und 1c beschreiben eine Aortenwurzel-Dilatation und unterteilen die Höhe der Dilatation von distal nach proximal (Ascendens, Sinus, Annulus). Typ 1d ist keine Aortendilatation, sondern eine Perforation einer Tasche.
Eine physiologische Aorteninsuffizienz ist im Gegensatz zur TR nicht typisch und sollte berichtet werden.
Die LV-Funktion und Größe sollte bei jeder Aorteninsuffizienz evaluiert und berichtet werden. Typischerweise kommt es bei einer chronischen Aorteninsuffizienz zu einer LV-Dilatation bei zunächst erhaltener Funktion, im Laufe der Zeit jedoch auch zur eingeschränkten Funktion. Die Angaben sollten auf Körperoberfläche indiziert erfolgen. Bei der volumetrischer Bestimmung ist wenn möglich eine 3D-Evaluation vorzunehmen. Bei eingeschränkten Sichtbedingungen kann KM zur Verbesserung eingesetzt werden.
Bei der akuten Aorteninsuffizienz kann es aufgrund des erhöhten LV-Drucks zu einem vorzeitigen Mitralklappenschluss kommen, der am besten im M-Mode (MV- Schluss vor der R-Zacke) dargestellt wird. Farnbdoppler-Methode ist nur eingeschränkt verwertbar.
2D-Bild. Die Anatomie (trikuspid, bicuspid) und Morphologie der Klappe (Verkalkungen, Perforationen, Prolaps, Flail ) sind zu beschreiben.
Die drei Komponenten des Jets (Konvergenzzone, Vena contracta, ventrikuläre Ausdehnung) sind im Farbdoppler darzustellen (Clip und Frame mit maximaler Ausdehnung). Hierzu sind Aufnahmen von apical und parasternal durchzuführen. Bei exzentrischen Jets ist v.a. die ventrikuläre Ausdehnung nicht zu verwerten.

Der Quotient Jetbreite/LVOT ist in der PLAX im LVOT (Abstand von max 1 cm zur Vena contracta) zu evaluieren. Ein Quotient unter 25% spricht für eine leichtgradige AR, ein Quotient ab 65% für eine hochgradige AR. Bei multiplen und exzentrischen Jets kann der Quotient nicht verwendet werden.
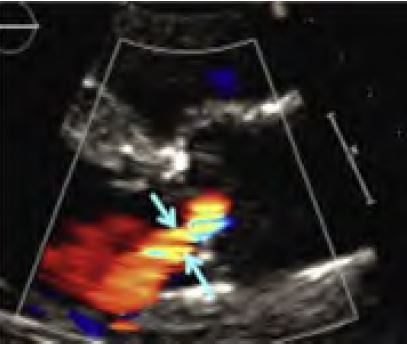
Die Vena contracta sollte in der PLAX im Zoom-Modus dargestellt werden. Eine VC unter 0,3 cm spricht für eine leichtgradige, eine VC über 0,6 für eine hochgradige AR. Bei guter Einstellung kann dieser Parameter auch bei exzentrischen Jets verwendet werden. Es besteht im Vergleich zu anderen Parameter eine relativ geringe Abhängigkeit von hämodynamischen Voraussetzungen. Auf eine exakte Messung ist zu achten, da aufgrund der kleinen Werte bereits kleine Fehler grosse Auswirkungen auf die Einordnung haben können. Nur wenn eine Konvergenzzone im normalen Nyquistbereich dargestellt werden kann, ist die Messung der VC valide. Eine Addition mehrere Jets ist nicht möglich.
Die Flusskonvergenz-Zone ist in der PLAX oder im 3C-Bick darzustellen. Zur Bestimmung des PISA-Radius ist der Zoom-Modus zu verwenden. Die Nulllinie wird in Richtung des Jets verschoben so dass ein Nyquistgrenze von 0,3 m/s eingestellt ist. Eine EROA ab 0,3 cm2 und ein Regurgitationsvolumen über 60 ml sprechen für eine hochgradige Aorteninsuffizienz.
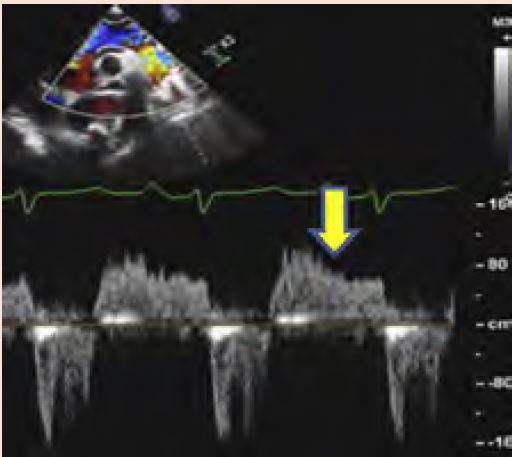
Diastolsche Flussumkehr. Zur Ermittlung der diastolischen Flussumkehr ist in der suprasternalen Anlotung ein pw-Doppler-Signal in der Aorta descendens abzuleiten. Ein holodiastolischer Fluss in der Aorta thoracalis deutet auf eine mind. mittelgradige AR hin, ein solches in der Aorta abdominalis legt das Vorliegen einer hochgradigen AR nahe. Differentialdiagnostisch sind Compliancestörungen bei älteren Patienten, AV-Fistel, und rupturierter Sinus valsalva auszuschließen. Bei akuten Formen (schneller Druckangleich) und Bradykardien (lange Diastole) kann das Flussumkehr falsch vermindert oder verkürzt sein. Eine kurze frühdiastolische Flussumkehr ist nicht pathologisch.
Regurgitationsvolumen. Das Regurgitationsvolumen wird bestimmt durch Abzug des effektiven Schlagvolumens, das an der gesunden PV oder MV evaluiert werden kann), vom totalen Schlagvolumen. Das totale Schlagvolumen kann volumetrisch oder über Dopplermessung am LVOT evaluiert werden. Der Ermittlung des RVol ist sehr fehleranfällig. Die EROA ergibt sich aus dem Quotient RVol/VTI),
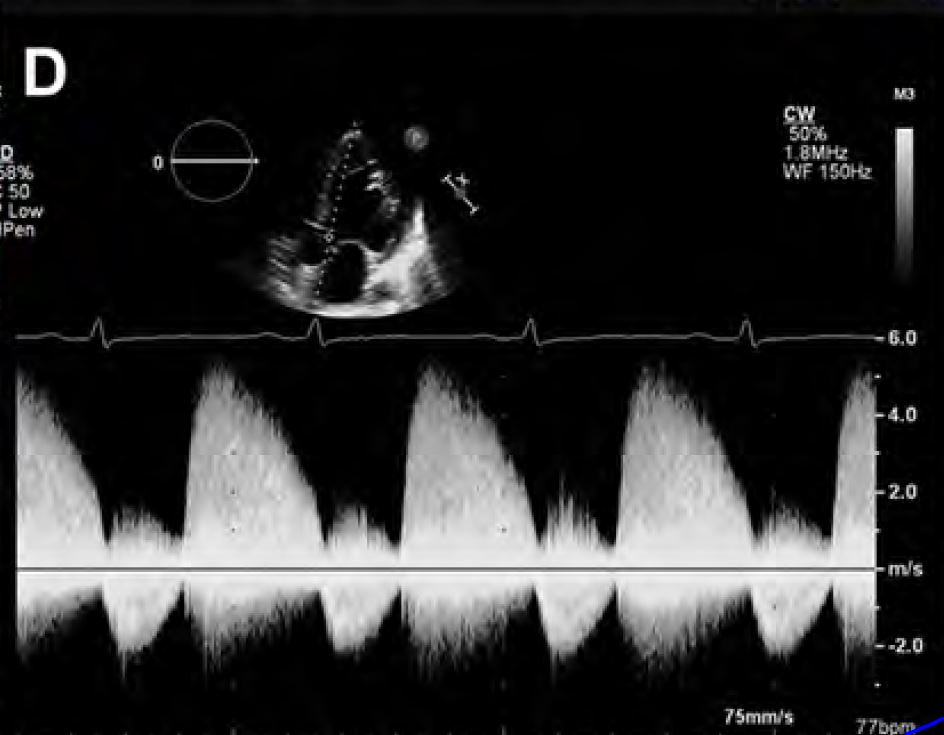
CW-Doppler. Bei der Ableitung des CW-Doppler-Signals schliesst ein dichtes Signal eine leichtgradige, ein unterbrochenes oder schwaches Signal eine hochgradige AR aus. Eine PHT über 500 msec spricht für eine leichtgradige, eine PHT unter 200 msec für eine hochgradige AR. Bei chronischen kompensierten AR kann durch die PHT eine Unterschätzung, bei einer diastolischen Funktonsstörung eine Überschätzung der AR auftreten. Vasodilatatoren führen ebenfalls zu einer Unterschätzung durch PHT wegen des verminderten LV-Drucks.
TEE. Eine TEE muss nur dann ergänzend durchgeführt werden, wenn die Morphologie der Klappe (z.B. Vegetationen) und der Aorta mittels TTE nicht hinreichend evaluiert werden können.
Integrativer Ansatz zur Schweregradeinteilung. Der Algorithmus der Leitlinien zur Schweregradbestimmung empfiehlt, zunächst leicht- und hochgradige AR zu identifizieren. Hierzu werden semiquantitative und qualitative Parameter empfohlen. Wenn sich daraus keine leicht- oder hochgradige AR ergibt, sollten die quantitative Parameter EROA, RVOL und RF hinzugezogen werden.

Es wird eine Einteilung in 4 Schweregrade empfohlen: Grad 1 leichtgradig, Grad 2 mittelgradig, Grad 4 hochgradig. Grad 3 wird in Abhängigkeit der Parameter in mittel- oder hochgradig eingeteilt.
Eine leichtgradige Aorteninsuffizienz liegt vor, wenn mind. 4 der folgenden Bedingungen vorliegen: 1) VC unter 3mm, 2) Jetbreite/LVOT unter 25%, 3) kaum sichtbare Flusskonvergenzzone, 4) sxchwaches oder unterbrochenes CW-Signal, 5) PHT über 500 msec, 6) LV nicht dilatiert. Die verwendeten Parameter sollten im Befund aufgeführt werden.
Eine hochgradige Aorteninsuffizienz liegt vor, wenn mind. 4 der folgenden Kriterien vorliegen: 1) Flail, 2) VC über 6mm, 3) Jetbreite 65% des LVOT, 4) PHT unter 200ms, 5) Holodiastolische Flussumkehr in der Aorta descendens, 6) LV dilatiert bei normaler Funktion. Liegt nach Evaluation der quantitativen Parametern Grad 3 vor, so erfolgt bei Vorliegenden von mind. 3 dieser Parameter ebenfalls die Einstufung in hochgradig, bei weniger als 3 dieser Parameter die Einstufung in mittelgradig. Alle verwendeten Parameter sollten im Befund aufgeführt werden.
Quantitative Parameter. Wenn die Evaluation der Parameter keinen eindeutigen Schweregrad nahelegt, sollte nach Vorliegen der quantitativen Parametern folgende Einteilung durchgeführt werden. Grad 1 wenn RVOL/RF/EROA unter 30 ml/30%/0,1, Grad 2 unter45ml /40%/0,2 cm2, Grad 3 unter 60 ml/50%/0,3cm2. Grad 4 ab 60ml/50%/0,3cm2.
Baumgartner, Helmut; Hung, Judy; Bermejo, Javier; Chambers, John B.; Edvardsen, Thor; Goldstein, Steven et al. (2017): Recommendations on the echocardiographic assessment of aortic valve stenosis: a focused update from the European Association of Cardiovascular Imaging and the American Society of Echocardiography. In: European heart journal cardiovascular Imaging 18 (3), S. 254–275.

